
新原料注册流程
注册流程:
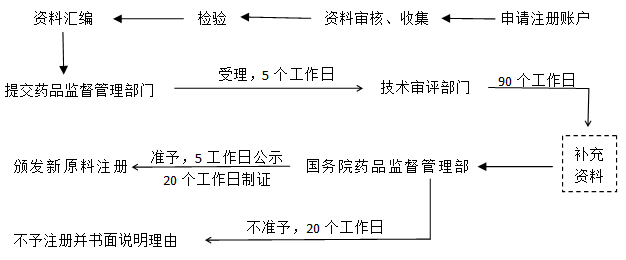
备案流程:

注册或者备案申请人主体资格
新原料注册人、备案人应当具备下列基本条件:具有与新原料相适应的不良反应监测和评价体系。
新原料注册人、备案人为境外企业的,应当指定我国境内的企业法人作为境内责任人。境内责任人应当履行以下义务:
(一)以注册人、备案人的名义,办理化妆品新原料注册、备案;
(二)协助注册人、备案人开展化妆品新原料安全监测与报告工作;
(三)协助注册人、备案人实施化妆品新原料召回工作;
(四)按照与注册人、备案人的协议,对投放境内市场的化妆品新原料承担相应的质量安全责任;
(五)配合药品监督管理部门的监督检查工作。
申请化妆品新原料注册或备案,提交下列资料:
1. 注册申请人、备案人和境内责任人的名称、地址、联系方式;
2. 新原料研制报告;
3. 新原料的制备工艺、稳定性及其质量控制标准等研究资料;
4. 新原料安全评估资料。
综普提供的服务
1. 根据申请人提供的新原料基本信息、研发背景、研发目的、新研究进展,协助完成新原料研制报告编写;
2. 指导申请人编制新原料制备工艺;
3. 指导申请人编制质量控制标准,包括稳定性试验数据、质量规格指标及其检验方法、可能存在的安全性风险物质及其控制等资料;
4. 指导申请人对新原料进行毒理学试验并编制毒理学安全性评价资料,安全性评估资料。
5. 收集新原料功能依据的相关资料,包括科学文献、法规资料、体外或动物试验研究数据、人体功能性评价试验资料等;
6. 指导申请人编制新原料技术要求。
7. 原料注册、备案全程代理服务